مروری کوتاه بر پسوریازیس
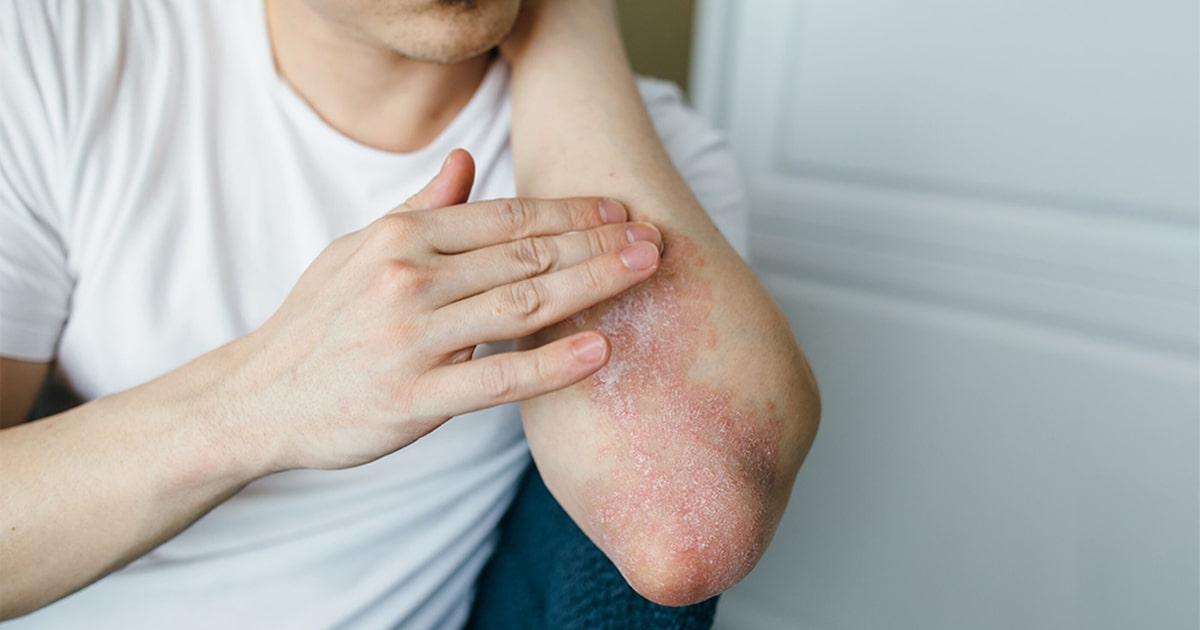
پسوریازیس یک بیماری پوستی مادام العمر متفاوت بالینی است که به اشکال مختلف مانند پلاک، معکوس، خالدار، پوسچولار یا اریترودرمیک ظاهر میشود. تخمین زده میشود که 60 میلیون نفر در سراسر جهان به پسوریازیس مبتلا هستند. حدود 1.52٪ از جمعیت در بریتانیا مبتلا به این بیماری هستند.
پسوریازیس یک بیماری التهابی با واسطه ایمنی است که یک جزء ژنتیکی اصلی دارد. ارتباط آن با آرتریت پسوریاتیک و افزایش میزان بیماریهای قلبی متابولیک، کبدی و روانی نیازمند یک رویکرد مراقبتی جامع و چند رشتهای است. درمان پسوریازیس شامل الف) داروهای موضعی : آنالوگهای ویتامین D و کورتیکواستروئیدها ب) فتوتراپی (اشعه ماوراء بنفش B باند باریک (NB-UVB) و اشعه پسورالن و اشعه فرابنفش (PUVA) Aج) درمان سیستمیک استاندارد (متوترکسات، سیکلوسپورین و آسیترتین) د) درمان بیولوژیک (فاکتور نکروز تومور) (TNF)، مهارکنندههای اینترلوکین IL -17 و IL-23 یا درمان های مهارکننده مولکول کوچک (دی متیل فومارات و آپرمیلاست). پیشرفت در درک پاتوفیزیولوژی آن منجر به توسعه درمان های بسیار موثر و هدفمند شده است.
- پسوریازیس یک بیماری پوستی مادام العمر متفاوت بالینی است که به اشکال مختلف مانند پلاک، معکوس، خالدار، پوسچولار یا اریترودرمیک ظاهر میشود.
- پسوریازیس دارای یک جزء ژنتیکی اصلی است که وراثت پذیری آن بین 60 تا 90 درصد تخمین زده میشود.
- درمان نواحی پسوریازیس شامل پوست سر، صورت، ناخن ها، اندام تناسلی، کف دست و کف پا دشوار است.
- شناخت و مدیریت بیماریهای همراه (مانند آرتریت پسوریاتیک، بیماری های روانی، قلبی عروقی و کبدی) بخش اساسی مراقبت های جامع برای افراد مبتلا به پسوریازیس است.
-
درمان پسوریازیس شامل الف) داروهای موضعی : آنالوگ های ویتامین D و کورتیکواستروئیدها ب) فتوتراپی (اشعه ماوراء بنفش B باند باریک (NB-UVB) و اشعه پسورالن و اشعه فرابنفش (PUVA) Aج) درمان سیستمیک استاندارد (متوترکسات، سیکلوسپورین و آسیترتین) د) درمان بیولوژیک (فاکتور نکروز تومور) (TNF)، مهارکنندههای اینترلوکین IL -17 و IL-23 یا درمانهای مهارکننده مولکول کوچک (دی متیل فومارات و آپرمیلاست). پیشرفت در درک پاتوفیزیولوژی آن منجر به توسعه درمان های بسیار موثر و هدفمند شده است.
مقدمه
پسوریازیس یک بیماری التهابی پوستی خود ایمنی مادام العمر است که با عوارضی مانند آرتروپاتی پسوریاتیک، بیماری های روانی، قلبی عروقی و کبدی همراه است. در سال 2014، سازمان بهداشت جهانی پسوریازیس را به عنوان یک بیماری غیرواگیر جدی به رسمیت شناخت و ناراحتی ناشی از تشخیص اشتباه، درمان ناکافی و… این بیماری را برجسته کرد. تخمین زده شده است که در جهان پسوریازیس 5.6 میلیون سال زندگی با ناتوانی تمام سنی را در سال 2016 به خود اختصاص داده است، این میزان حداقل سه برابر بیماری التهابی روده است.
اپیدمیولوژی
پسوریازیس هم مردان و هم زنان را تحت تأثیر قرار میدهد و در زنان و کسانی که سابقه خانوادگی دارند زودتر شروع میشود. سن شروع آن یک توزیع دو وجهی را نشان میدهد که اوج آن در 30-39 سال و 60-69 سال در مردان و 10 سال زودتر در زنان است. تخمین زده میشود که 60 میلیون نفر در سراسر جهان به پسوریازیس مبتلا هستند، با شیوع خاص کشور بین 0.05٪ از جمعیت در تایوان و 1.88٪ در استرالیا متفاوت است. این بیماری در مناطق پردرآمد و مناطق با جمعیت مسنتر شایعتر است. در بریتانیا، 1.52٪ از جمعیت عمومی را تحت تاثیر قرار میدهد.
سبب شناسی
پاتوژنز پسوریازیس چند عاملی است و ژنتیک یکی از عوامل اصلی به ویژه در افرادی است که پسوریازیس پلاکی زودرس (کمتر از 40 سال) دارند. این مورد در مطالعات دوقلو، مبتنی بر خانواده و در مقیاس بزرگ در سطح جمعیت، با وراثت پذیری 60-90٪ نشان داده شد. در حال حاضر بیش از 60 جایگاه حساسیت با استفاده از مطالعات ارتباطی گسترده ژنوم شناسایی شده است. بسیاری از ژنهای علت کاندید در ارائه آنتی ژن (HLA-C و ERAP1)، سیگنال دهی NF-kappa B (TNIP1)، مسیر اینترفرون نوع 1 مسیر RNF113 وIFIH1، اینترلوکین (IL)-23/Th17 (IL23R، IL12B و TYK2) و عملکرد سد پوست (LCE3) هستند. در اتیولوژی پسوریازیس یک فعل و انفعال پیچیده بین سلول های T، سلول های دندریتیک و کراتینوسیتها به عنوان عامل اصلی پاتوفیزیولوژی پسوریازیس است، با محور IL-23/Th17 که محرک اصلی فعال سازی ایمنی، التهاب مزمن و تکثیر کراتینوسیت است. محرکهای محیطی تشدید کننده پسوریازیس مانند چاقی، استرس، بتابلوکرها، سیگار کشیدن و لیتیوم شناخته شده اند. اگرچه اطلاعات کمی وجود دارد، به نظر میرسد که پسوریازیس پوسچولار از نظر ژنتیکی متمایز است و ژنهای حساسیت متفاوتی در آن نقش دارند(IL36RN، AP1S3 در ژنهای اروپایی تبار و CARD14).
تظاهرات بالینی
پسوریازیس به شکلهای مختلفی مانند پلاک، معکوس، خالدار، پوسچولار یا اریترودرمیک ظاهر می شود. شایعترین شکل پسوریازیس پلاکی است که به صورت پلاکهای صورتی ماهی سالمون کاملاً مشخص با ظاهر سفید نقرهای، معمولاً در یک توزیع متقارن ظاهر میشود و سطوح بازکننده (بهویژه آرنج و زانو)، تنه و پوست سر را تحت تأثیر قرار میدهد (شکل 1). نقاط خونریزی ممکن است در جایی که فلسها برداشته شدهاند نشانه آسپیتز (Auspitz’sSign) مشخص شود. پسوریازیس معکوس یا فلکسور بدون پوسته ریزی زیاد ظاهر میشود و ممکن است زیر بغل، زیر پستان و نواحی تناسلی را درگیر کند. پسوریازیس خالدار باعث فوران متقارن حاد پاپول ها/پلاک های قطره مانند می شود که عمدتاً تنه و اندام ها را درگیر میکند، که به طور کلاسیک اما همیشه با عفونت استرپتوکوکی رخ نمیدهد.
بیماران مبتلا به پسوریازیس ممکن است بعداً به پسوریازیس پلاکی مبتلا شوند. در موارد نادر بیماری شدید کنترل نشده، پسوریازیس باعث ایجاد بثورات اریتماتوز گسترده (اریترودرمی) میشود که به دلیل عوارض بالقوه از جمله هیپوترمی، خطر عفونت، آسیب حاد کلیه و نارسایی قلبی با برون ده بالا، تهدید کننده زندگی است. پدیده کوبنر ظهور پسوریازیس را در نواحی پوستی که تحت تأثیر تروما قرار گرفته اند توصیف میکند.
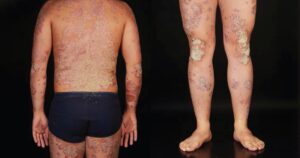
شکل 1. پسوریازیس پلاکی مزمن. پلاک های اریتماتوز گسترده، متقارن توزیع شده و به خوبی مشخص شده اند. سطوح اکستانسور (پشت دست و پا) مانند آرنج و زانو معمولاً تحت تأثیر قرار گرفته اند.
ناخنها ممکن است در 50 درصد بیماران تحت تاثیر قرار گیرند و ممکن است به صورت فرورفتگی ناخن (تورفتگی در ناخن)، اونیکولیز (جدایی صفحه ناخن از بستر ناخن)، لکه های چربی (تغییر رنگ بستر ناخن)، دیستروفی و هیپرکراتوز زیر ناخن ظاهر شوند.
حضور چند بیماری همزمان و پسوریازیس
مولتی موربیدیتی که به عنوان وجود دو یا چند بیماری مزمن تعریف میشود، در افراد مبتلا به پسوریازیس رایج است. آرتریت پسوریاتیک (PsA) تا 30 درصد بیماران مبتلا به پسوریازیس را تحت تأثیر قرار میدهد، این بیماری در بیماران مبتلا به دیستروفی ناخن و پسوریازیس پوست سر، اینترگلوتئال، پرینال شایعتر است. در اکثر بیماران، پسوریازیس تا 10 سال قبل از بیماری مفصلی ایجاد میشود. بنابراین، پزشکان عمومی و متخصصین پوست که از بیماران مبتلا به پسوریازیس مراقبت میکنند، برای تشخیص زودهنگام PsA آرتریت پسوریاتیک در موقعیت مناسبی قرار دارند. برای غربالگری PsA، یک پرسشنامه معتبر پنج سوالی، ابزار غربالگری اپیدمیولوژی پسوریازیس (PEST) توصیه میشود. افراد مبتلا به پسوریازیس بیشتر از افراد عادی از چاقی، بیماریهای قلبی عروقی، بیماری کبد چرب غیر الکلی، دیابت و سندرم متابولیک رنج میبرند، که این میزان به ویژه در افراد مبتلا به پسوریازیس شدیدتر افزایش مییابد. این امر ممکن است با ویژگیهای ژنتیکی مشترک، مسیرهای التهابی بیماریزا و عوامل خطر مشترک مرتبط باشد. پیامد آن افزایش نرخ مرگ و میر در بیماران مبتلا به پسوریازیس شدید است که در درجه اول به دلایل قلبی عروقی است. علاوه بر این، میزان اختلالات سلامت روان (مانند اضطراب و افسردگی) نیز در مقایسه با جمعیت عمومی افزایش یافته است که تأثیر روانی اجتماعی پسوریازیس را برجسته میکند.
ارزیابی بیماران مبتلا به پسوریازیس
پسوریازیس بر اساس میزان درگیری پوست (مساحت سطح بدن (BSA)) و شدت اریتم، سفتی و پوسته پوسته شدن ارزیابی میشود. در مراقبتهای ثانویه، نمرات معتبر مانند شاخص شدت ناحیه پسوریازیس (PASI) و مقیاس ارزیابی جهانی پزشک به طور معمول همراه با معیارهای پیامد گزارش شده توسط بیمار مانند شاخص کیفیت زندگی درماتولوژی (DLQI) استفاده می شود. توجه به تأثیر روانشناختی آن ضروری است زیرا ممکن است به عدم مشارکت و عدم پایبندی به درمان کمک کند. هر برخورد بیمار فرصتی برای غربالگری چند بیماری است. علاوه بر بهبود سلامت کلی، تشخیص بیماریهای چندگانه ممکن است بر انتخاب درمان پسوریازیس تأثیر بگذارد. برای مثال، بیماری مزمن کبدی ممکن است مصرف متوترکسات را منع کند. بنابراین، رویکرد چند رشتهای بسیار مهم است و اغلب شامل روماتولوژیستها، متخصصان گوارش و بیماری های کبدی و روانشناسان بالینی میشود.
درمان پسوریازیس
گزینههای درمانی پسوریازیس شامل درمان موضعی، فتوتراپی یا درمان سیستمیک است و در دستورالعملهای مؤسسه ملی بهداشت و مراقبت عالی بریتانیا (NICE) خلاصه شده است. اهداف درمانی شامل حداقل 75% یا 90% بهبود در PASI (PASI75 یا PASI90) کمک کننده است. درمان های موضعی مانند آنالوگ های ویتامین D (کلسی پوتریول) یا کورتیکواستروئیدها خط اول هستند. اثربخشی درمان موضعی را میتوان با درمان ترکیبی (مانند کلسیپوتریول/بتامتازون) افزایش داد. دیترانول و تار که قبلاً محبوب بود، کمتر مورد استفاده قرار میگیرند، زیرا پوست را لکهدار و تحریک میکرد. پسوریازیس در محلهای درمان دشوار (پوست سر، صورت، ناخنها، اندام تناسلی، کف دست و پا) به دلیل تأثیر عمیق آن بر عملکرد و پاسخ نسبتاً ضعیف به درمان، توجه ویژهای را ضروری میکند (شکل 2). استفاده از استروئیدها برای صورت یا اندام تناسلی به دلیل خطر آتروفی پوست و تلانژکتازی باید دارای قدرت کم و محدود به استفاده کوتاه مدت باشد.
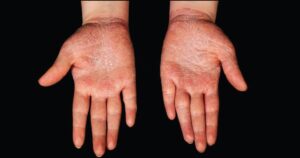
شکل 2. پسوریازیس که کف دست را تحت تاثیر قرار می دهد. درمان پسوریازیس در کف دست، کف پا، پوست سر، صورت، ناخن ها و اندام تناسلی دشوار است و ممکن است تأثیر عمیقی بر فعالیت های روزمره داشته باشد.
درمان خط دوم شامل فتوتراپی (اشعه ماوراء بنفشB باند باریک (NB-UVB) و پسورالن با اشعه ماوراء بنفش A (PUVA)) و عوامل سیستمیک معمولی (متوترکسات، سیکلوسپورین و آسیترتین) است. NB-UVB به دلیل خطرات سرطان پوست با دوزهای تجمعی PUVA تا حد زیادی جایگزین PUVA شده است. متوترکسات با مهار لنفوسیت ها از طریق مکانیسم های متعددی از جمله مهار دی هیدروفولات ردوکتاز، محاصره آمینو ایمیدازول کربوکسامید ریبوتید ترانسفورمیلاز (AICARTase) و تجمع آدنوزین عمل می کند. جدیترین اثر نامطلوب آن سرکوب مغز استخوان است. سایر عوارض بالقوه درمان عبارتند از تهوع، پنومونیت، هپاتیت، فیبروز کبد و اثرات تراتوژن است. متوترکسات معمولاً هر هفته به صورت خوراکی مصرف میشود. فرمولاسیون زیر جلدی عوارض جانبی گوارشی کمتری ایجاد میکند و به دلیل فراهمی زیستی بیشتر، مؤثرتر است. سیکلوسپورین یک مهارکننده کلسینورین است و شروع سریع اثر دارد، اما ممکن است باعث فشار خون بالا و مسمومیت غیرقابل برگشت کلیوی شود. آسیترتین یک رتینوئید خوراکی است که باعث تمایز کراتینوسیتها میشود. عوارض جانبی احتمالی آن شامل خشکی پوست، ریزش مو، افزایش چربی خون و سمیت کبدی است. متوترکسات و آسیترتین در بارداری منع مصرف دارند. برای بیماری های مقاوم به متوترکسات و یا سیکلوسپورین یا در مواردی که درمان های خط دوم مناسب نیستند، ممکن است درمانهای بیولوژیک یا مهارکنندههای مولکول کوچک خوراکی در نظر گرفته شود. درمانهای بیولوژیکها آنتی بادیهای مونوکلونال یا گیرندههای محلول هستند که سیتوکینهای پیش التهابی را هدف قرار میدهند. آنها تأثیر چشمگیری بر پیامدهای بیماری متوسط تا شدید داشتهاند.
در حال حاضر 4 مدل بیولوژیک موجود است:
• مسدود کنندههای فاکتور نکروز تومور آلفا (TNF-alpha)
• مهارکنندههای اینترلوکین 12 و 23 (IL-12/23).
• مهارکنندههای IL-17
• مهارکنندههای IL-23
هر یک از این مولکولها پیام رسانهای خاصی در سیستم ایمنی بدن هستند که در ایجاد پسوریازیس نقش دارند. دوز و عوارض جانبی بسته به نوع دارو متفاوت است.
مسدود کنندههای TNF-alpha شامل آدالیموماب (Humira)، اتانرسپت (Enbrel) و certolizumab pegol (Cimzia) هستند.
همه آنها برای درمان پسوریازیس و آرتریت پسوریاتیک تایید شدهاند. بسته به نوع دارو، افراد هر هفته یا هر هفته به یک دوز نیاز دارند. همچنین، این بیولوژیکها گستردهترین داروها هستند، زیرا TNF-alpha یک واسطه بالادستی التهاب است. هرچه هدف در پاییندستتر باشد، بیولوژیک خاصتر است و – به طور بالقوه – عوارض جانبی کمتری دارد. تنها مهارکننده IL-12/23 موجود، ustekinumab (Stelara) است. این میتواند پسوریازیس و آرتریت پسوریاتیک را درمان کند و فرد هر 12 هفته یک دوز از آن را دریافت میکند. مهارکنندههای IL-17 شامل سکوکینوماب (Cosentyx)، ایکسکیزوماب (Taltz) و برودالوماب (Siliq) هستند. آنها هم پسوریازیس و هم آرتریت پسوریاتیک را درمان میکنند و برنامه دوز هر 2 تا 4 هفته است. مهارکنندههای IL-23 جدیدترین کلاس بیولوژیک هستند که وارد بازار شدهاند. آنها عبارتند از risankizumab-rzaa (Skyrizi)، guselkumab (Tremfya) و tildrakizumab-asmn (ایلومیا). هر کدام برای درمان پسوریازیس تایید شده اند. بسته به دارو، فرد هر 8 تا 12 هفته یک دوز دریافت می کند. هیچ درمان واحدی به عنوان بهترین درمان وجود ندارد و انتخاب بیولوژیک باید متناسب با نیازهای هر بیمار باشد.
در حال حاضر، این در درجه اول تحت تأثیر اطلاعات بالینی مانند عوامل پسوریازیس (فنوتیپ بیماری و حضور PsA و نتایج درمان بیولوژیک قبلی)، بیماریهای همراه (بیماری دمیلینه کننده و بیماری التهابی روده)، عوامل خاص دارو (تکرار دوز) و ملاحظات سبک زندگی (بارداری) است. اطلاعات ژنومی این پتانسیل را دارد که به کارگیری موثر درمان ها در آینده را هدایت کند، و این زمینه تحقیقات فعال است. اگرچه داروهای بیولوژیک بسیار موثر هستند، اما نیاز به تجویز منظم زیر جلدی یا داخل وریدی دارند.
مهارکنندههای کوچک مولکول خوراکی از جمله آپرمیلاست (مهارکننده فسفودی استراز 4) و متیل فومارات برای استفاده در پسوریازیس متوسط تا شدید مجوز دارند، و آزمایشها برای مولکولهای کوچک مسدودکننده تیروزین کیناز 2 در Janus kinase (JAK) مبدل سیگنال و فعال کننده پروتئینی مسیر نسخه برداری ادامه دارد.
پسوریازیس پوسچولار
پسوریازیس پوسچولار یک فنوتیپ متمایز است که با پوسچولهای استریل مشخص میشود که میتواند حاد ژنرالیزه( پسوریازیس پوسچولار عمومی(GPP) یا محدود به انگشتان (ACH) یا کف دست و پا (پوستولوز کف پلانتار باشد. GPP می تواند به صورت حاد با فوران گسترده جوش های سطحی و پوست اریتماتوز ظاهر شود. بیماران ممکن است با تب ناخوشایند باشند، و آزمایشهای خون معمولاً نوتروفیلی و نشانگرهای التهابی بالا را نشان میدهند. در حالی که پسوریازیس پوسچولار عمومی میتواند تهدیدکننده زندگی باشد، پوسچولوز موضعی نیز میتواند به شدت بر فعالیتهای روزانه تأثیر بگذارد.
علیرغم وجود درمان های رو به رشد درمان برای پسوریازیس پلاکی، درمان موثر پسوریازیس پوسچولار همچنان منطقه ای با نیازهای برآورده نشده است. پوسچولوز کف پلانتار و آکرودرماتیت پیوسته هالوپو به درمان هایی که در پسوریازیس پلاکی استفاده میشود سرکش هستند. استروئیدهای موضعی قوی با انسداد خط اول هستند. PUVA ممکن است در پوسچولوز کف پا در نظر گرفته شود، اما درمانهای سیستمیک اغلب مورد نیاز است. پیشرفتها در درک ما از نقش بیماریزای جهشهای IL36RN در GPP نیز منجر به توسعه مهارکنندههای گیرنده IL-36 شده است که آزمایشها در حال انجام است. به طور چکیده، پسوریازیس یک بیماری التهابی شایع پوستی است که عمدتاً ژنتیکی است و با عوارض پزشکی و روانی اجتماعی قابل توجهی همراه است. پیشرفتها در درک پاتوفیزیولوژی آن منجر به افزایش تعداد گزینههای درمانی شده است که میتواند زندگی افراد مبتلا به پسوریازیس را به طور چشمگیری بهبود بخشد.