لیگاند OX40L رهبر ارکستر سمفونی التهابی درماتیت آتوپیک
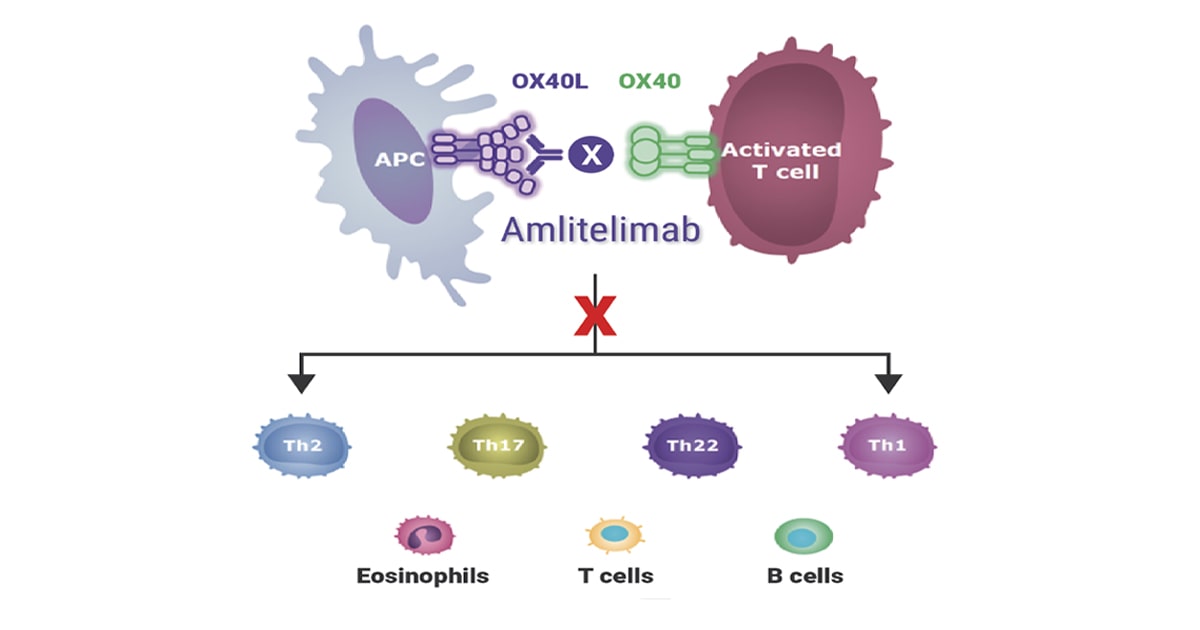
درماتیت آتوپیک (AD) یک بیماری مزمن التهابی پوستی است که دارای پاتوفیزیولوژی پیچیدهای میباشد و شامل اختلالات ایمنی و نقص در سد پوستی است. علائم و نشانههای AD نتیجه التهاب موضعی و سیستمیک ناشی از سلولهای T است. فعالسازی و گسترش زیرمجموعههای سلولهای T موثر، از جمله سلولهای T کمککننده 2 (Th2)، Th1، Th17 و Th22، باعث ایجاد التهاب ناهمگن و مشخصه AD میشود. این سلولهای T فعال، سایتوکاینهای التهابی مانند اینترلوکین 4 (IL-4)، IL-13، IL-17 و IL-31 را آزاد میکنند که به اختلال در سد پوستی، ضخیم شدن اپیدرم و خارش مشاهدهشده در AD منجر میشوند. OX40-لایگاند (OX40L) یک مولکول سیگنالدهی کمکی القایی در مسیر بالا دست است که به گیرنده خود (OX40) بر روی سلولهای T فعال متصل میشود و با تشویق تکثیر، افزایش بقا و آزادسازی سایتوکاینها، گسترش سلولهای T موثر را تنظیم میکند. مشاهده افزایش بیان OX40L، گیرنده آن (OX40) و تعداد سلولهای بیانکننده OX40 در پوست مبتلایان به AD در مقایسه با پوست سالم، نشاندهنده این است که این مسیر سیگنالدهی القایی به التهاب پاتولوژیک AD کمک میکند. در اینجا، نقش OX40L در ایجاد و پایداری مزمن AD را بررسی میکنیم.
معرفی سمفونی التهابی: با هدایت OX40L و سلولهای ارائهدهنده آنتیژن
همانطور که با هدایت رهبر ارکستر، سازهای ویولن، ویولا، ویولنسل و سازهای بادی در کنار هم برای تقویت صدای خود عمل میکنند، سلولهای سیستم ایمنی نیز فعال میشوند تا نمره التهابی را که عامل AD است، تقویت کنند.
رهبر – سلولهای حرفهای ارائهدهنده آنتیژن (APCs) و OX40L
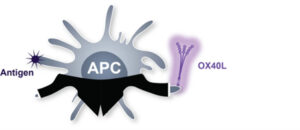
سلولهای حرفهای ارائهدهنده آنتیژن (APCs) مانند سلولهای دندریتیک، ماکروفاژها و سلولهای B را بهعنوان رهبران سیستم ایمنی تصور کنید. همانطور که یک رهبر ارکستر نتهای موسیقی را تفسیر میکند و ارکستر را هدایت میکند، APCها مواد خارجی مانند آلرژنها را پردازش کرده و پاسخ التهابی هدفمند را از طریق ارائه قطعات پردازششده آلرژن به سلولهای T نابالغ با استفاده از کمپلکس سازگاری بافتی اصلی (MHC) کلاس II آغاز میکنند.
APCها از طریق بیان چندین مولکول همتحریکی (پروالتهابی) و هممهاری (ضدالتهابی) که بهعنوان مولکولهای نقطه کنترل ایمنی شناخته میشوند و میزان فعالسازی سلولهای T را تنظیم میکنند، یک پاسخ التهابی را هدایت میکنند. OX40L یک مولکول همتحریکی است که عمدتاً توسط APCهای حرفهای فعالشده بیان میشود و بهعنوان بخشی از گسترش نقش رهبر عمل میکند. OX40L همچنین توسط APCهای غیرحرفهای مانند سلولهای لنفوئیدی ذاتی نوع 2 (ILC2s)، سلولهای اندوتلیال و فیبروبلاستها که آنتیژنها را با استفاده از MHC کلاس I ارائه میکنند، بیان میشود. سیگنالهای OX40L به تنظیم و تقویت بیشتر پاسخ ایمنی کمک میکنند.
سازهای زهی – سلولهای T کمککننده موثر
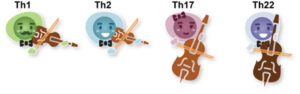
سلولهای T موثر مانند بخش سازهای زهی یک ارکستر هستند که اغلب ملودی اصلی را اجرا کرده و با سایر سلولهای ایمنی همنوازی میکنند تا پاسخ التهابی در درماتیت آتوپیک (AD) را پیش ببرند. همانطور که سازهای زهی مختلف صداهای متمایزی تولید میکنند، زیرمجموعههای سلولهای T کمککننده نیز سایتوکاینهای متنوعی آزاد میکنند که شدت و نوع پاسخ ایمنی را تعیین میکنند. مانند رهبری که بخش زهی را هدایت میکند، سلولهای حرفهای ارائهدهنده آنتیژن (APCs) فعالسازی و تمایز سلولهای T نابالغ را هدایت میکنند. این سلولهای T نابالغ به زیرمجموعههای تخصصی سلولهای T کمککننده – Th1، Th2، Th17، و Th22 – تمایز مییابند که هرکدام نقش منحصربهفردی در سمفونی التهاب AD ایفا میکنند. پس از فعالسازی، این زیرمجموعههای سلولهای T کمککننده موثر بیان OX40 را افزایش میدهند و آنها را برای دریافت سیگنالهای بقا، تکثیر و آزادسازی سایتوکاینها حساس میکنند.
سازهای بادی برنجی – سلولهای T حافظه

بیشتر سلولهای T کمککننده موثر دچار آپوپتوز میشوند؛ اما برخی از آنها به سلولهای T حافظه با عمر طولانی تبدیل میشوند. سلولهای T حافظه، مانند صدای قوی و جسورانهای که از سازهای بادی برنجی تولید میشود، با قرار گرفتن مجدد در معرض آنتیژنها، پاسخی سریعتر و قویتر را تسهیل میکنند و با بسیج سریع سایر سلولهای ایمنی، پاسخ التهابی سریعی را بهوجود میآورند.
سازهای کوبهای – سلولهای T تنظیمی (Tregs)

همانطور که سازهای کوبهای ساختار ریتمیک و لایههای پیچیدگی را به یک قطعه موسیقی اضافه میکنند، سلولهای T تنظیمی (Tregs) نیز پاسخ التهابی را تنظیم میکنند. آنها تضمین میکنند که پاسخ ایمنی بیش از حد آشفته یا شدید نشود و با حفظ تحمل ایمنی نسبت به آلرژنها و جلوگیری از آسیب بافتی، تعادل لازم را ایجاد میکنند.
حرکت اول – آغاز سیگنالدهی OX40L در درماتیت آتوپیک (AD)
مانند یک ابوا که نت تنظیم را مینوازد و آغاز سمفونی را اعلام میکند، نقص در سد پوستی در AD، نفوذ آلرژنها را ممکن میسازد. سپس آلرژنها توسط APCهای حرفهای پردازش و برای شناسایی توسط سلولهای T به نمایش گذاشته میشوند. پس از اتصال آنتیژن به گیرنده سلول T (TCR)، تعامل اولین جفت گیرنده−لیگاند همتحریکی که بر روی APCها و سلولهای T بیان میشود (مانند CD40−CD40L و CD28−B7) اتفاق میافتد. پیش از فعالسازی، APCها و سلولهای T نابالغ بهطور عمومی OX40L یا OX40 را بیان نمیکنند. این فعالسازی اولیه سلولهای T باعث شروع بیان مولکول همتحریکی ثانویه OX40L در سطح APCها در عرض 24 ساعت میشود. بیان گیرنده OX40 نیز به زودی پس از 1 تا 5 روز در سطح سلولهای T فعالشده رخ میدهد. اتصال OX40L به گیرندهاش سمفونی پویا پاسخ ایمنی را هدایت کرده و تکثیر و بقای سلولهای T و آزادسازی سایتوکاینها در AD را تقویت میکند.
چندین سیگنال میزان بیان OX40L را کنترل میکنند، از جمله تحریک آنتیژن، مسیرهای همتحریکی دیگر، و آلارمینهایی مانند تیمیک استرومال لنفوپوئیتین که از سلولهای اپیتلیال آسیبدیده آزاد میشوند. با سیگنالدهی OX40L، سلولهای T فعال بهصورت کلونی گسترش مییابند و به سلولهای T موثر تبدیل میشوند. این سلولهای T موثر، بهویژه سلولهای Th2، سایتوکاینهایی مانند IL-4 و IL-13 ترشح میکنند که بیان پروتئینهای ساختاری کلیدی در کراتینوسیتها مانند فیلاگرین و لوریکرین را کاهش میدهند. این کاهش، همراه با فیبروز ناشی از افزایش تولید کلاژن که توسط این سایتوکاینها تحریک میشود، سد اپیدرمی را تضعیف کرده و نفوذ آلرژنها را افزایش میدهد.
افزون بر این، سلولهای Th2 نیز IL-31 را آزاد میکنند، که یک محرک قوی خارش است. این تمایل غیرقابلمقاومت به خاراندن، سد اپیدرمی که از قبل آسیب دیده است را بیشتر تخریب میکند. التهاب ناشی از Th2 توسط سلولهای ایمنی دیگر که سایتوکاینهای نوع 2 تولید میکنند، از جمله سلولهای لنفوئیدی ذاتی نوع 2 (ILC2s) که OX40L را بیان میکنند و در تعداد زیادی در پوست مبتلایان به AD یافت میشوند، بیشتر تقویت میشود. این زنجیره پیچیده التهاب یک حلقه بازخورد قوی را به وجود میآورد. کراتینوسیتهای آسیبدیده آلارمینهای بیشتری آزاد میکنند که مسیر OX40L را فعال میکند و این به نوبه خود التهاب نوع 2 سلولهای T و التهاب غیر نوع 2 را تقویت و پایدار میسازد. تحت تأثیر سیگنالدهی OX40L، سمفونی التهابی AD به اوج خود میرسد و به یک وضعیت مزمن تبدیل میشود.
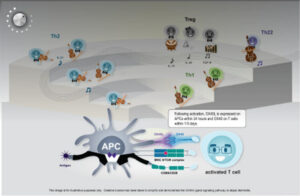
شکل ۱: APCهای حرفهای و OX40L برای فعالسازی و گسترش سلولهای T موثر در درماتیت آتوپیک (AD) حیاتی هستند.
پس از اتصال آنتیژن به گیرنده سلول T (TCR)، تعامل اولین جفت گیرنده-لیگاند همتحریکی که بر روی APCها و سلولهای T بیان میشود (مانند CD40−CD40L و CD80−CD28) رخ میدهد.
مرحله اولیه فعالسازی سلول T باعث بیان مولکول همتحریکی ثانویه OX40L در سطح APCها میشود. به زودی پس از آن، بیان گیرنده OX40 در سطح سلولهای T فعالشده انجام میگیرد.
سیگنالدهی OX40L باعث گسترش سلولهای T موثر شده و القای سلولهای T تنظیمی (Treg) را سرکوب میکند.
AD (درماتیت آتوپیک)، APC (سلول ارائهدهنده آنتیژن)، CD (خوشه تمایزیابی)، MHC II (کمپلکس سازگاری بافتی اصلی کلاس II)، OX40L (OX40-لایگاند)، TCR (گیرنده سلول T)، TGF-B (عامل رشد تغییر شکلدهنده بتا)، Th (سلول T کمککننده)، Treg (سلول T تنظیمی)
سمفونی گیر افتاده در فورتیسیمو – سیگنالدهی OX40L در مزمن شدن و بازگشت درماتیت آتوپیک (AD)
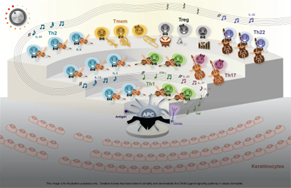 شکل ۲: ارکستر التهاب درماتیت آتوپیک (AD) تحت هدایت APC حرفهای و OX40-لایگاند:التهاب درماتیت آتوپیک (AD) تحت هدایت APCهای فعال و OX40L سازماندهی میشود.
شکل ۲: ارکستر التهاب درماتیت آتوپیک (AD) تحت هدایت APC حرفهای و OX40-لایگاند:التهاب درماتیت آتوپیک (AD) تحت هدایت APCهای فعال و OX40L سازماندهی میشود.
مانند سازهای زهی در ارکستر، پس از فعالسازی اولیه، سلولهای T موثر شامل Th2، Th1، Th17 و Th22، OX40 را بیان میکنند و آنها را نسبت به سیگنالهای رهبر ارکستر برای بقا، تکثیر و آزادسازی سایتوکاینها پاسخگو میسازد.
سیگنالدهی OX40L همچنین القای سلولهای T تنظیمی (Tregs) را سرکوب کرده و عملکرد سرکوبکننده ایمنی آنها را تضعیف میکند.
بقا طولانیمدت سلولهای T موثر که توسط سیگنالدهی OX40L القا میشود، به برخی از این سلولها اجازه میدهد که به سلولهای T حافظه استراحتکرده تبدیل شوند.
AD (درماتیت آتوپیک) ، APC (سلول ارائهدهنده آنتیژن) ، IFNγ (اینترفرون گاما) ، IL (اینترلوکین)، OX40L (OX40-لایگاند) ، Th (سلول T کمککننده) ، Tmem (سلول T حافظه) ، TNF (عامل نکروز تومور) ، Treg (سلول T تنظیمی)
ملودیهای ناسازگار آسیب اپیدرمی و اختلالات ایمنی، محیطی پیشالتهابی ایجاد میکنند که زمینهساز یک پاسخ التهابی طولانیمدت میشود. این محیط التهابی که تحت هدایت سیگنالدهی OX40L است، گسترش سلولهای Th2 را تقویت کرده و جذب سلولهای T موثر بیشتری را به محل آسیب تحریک میکند. در حالت مزمن AD، سایر زیرمجموعههای سلولهای T کمککننده، از جمله سلولهای Th1، Th17 و Th22 نیز به میکرو محیط التهابی جذب میشوند. این عوامل باعث افزایش شدت التهاب میشوند؛ به عنوان مثال، IL-22 که عمدتاً توسط سلولهای Th22 تولید میشود، با افزایش شدت AD مرتبط است و باعث تکثیر کراتینوسیتها شده که به ضخیم شدن اپیدرم (هایپرپلازی) که از ویژگیهای این بیماری است، منجر میشود.
نکته مهم این است که OX40L باعث تولید سلولهای T حافظه و مهار عملکرد سلولهای T تنظیمی (Tregs) میشود که این موضوع به پاتوفیزیولوژی AD کمک میکند. سیگنالدهی OX40L همچنین نشان داده است که باعث سرکوب القای Tregs میشود که از عملکرد سرکوبکننده ایمنی آنها میکاهد. بقا طولانیمدت سلولهای T موثر که توسط سیگنالدهی OX40L القا میشود، به برخی از این سلولها کمک میکند که به سلولهای T حافظه استراحتکرده تبدیل شوند. در AD، قرار گرفتن مجدد در معرض آنتیژنهای قبلی، باعث فعالسازی سریع سلولهای T حافظه استراحتکرده میشود. این سلولهای T حافظه سپس به سلولهای T حافظه موثر تبدیل شده و به سرعت OX40 را بیان میکنند. این فرآیند، آزادسازی سایتوکاینهای التهابی و گسترش سلولهای T حافظه موثر را تسهیل میکند. سلولهای T حافظه موثر که OX40 را بیان میکنند، در ضایعات AD افزایش مییابند. این موضوع نشان میدهد که محور سیگنالدهی OX40L نقش مهمی در عود بیماری در AD ایفا میکند.
حرف آخر
APCها و سلولهای T نابالغ بهطور گسترده OX40L یا OX40 را بیان نمیکنند؛ بلکه بیان OX40L و OX40 پس از فعالسازی سلولها القا میشود. پس از القا، سیگنالدهی OX40L بهعنوان یک مسیر سیگنالدهی اصلی در مسیرهای متعدد ایمنی عمل میکند و به چرخه اختلال اپیدرمی و التهاب در پاتوفیزیولوژی AD کمک میکند. AD یک بیماری التهابی پویا و ناهمگن است که شامل فعالسازی APCها و گسترش زیرمجموعههای مختلف سلولهای T کمککننده میشود. مسیر OX40L القای Tregs را سرکوب کرده و در عین حال گسترش زیرمجموعههای سلولهای T کمککننده خاص آنتیژن را تقویت میکند. این سلولهای T کمککننده سایتوکاینهایی تولید میکنند که علائم سنگین و آزاردهنده AD را میانجیگری میکنند. علاوه بر این، مسیر سیگنالدهی به تولید سلولهای T حافظه کمک میکند که ممکن است بازگشت AD را امکانپذیر سازد. با توجه به پیچیدگی التهاب زیرساختی در بیماران مبتلا به AD، درک بیشتر مسیر OX40L میتواند به بهبود شناخت ما از پاتوفیزیولوژی AD کمک کند. در حال حاضر، درمانهای تأیید شده عمدتاً مسیرهای خاص سایتوکاین را هدف قرار میدهند؛ اما ناهمگنی AD نیاز به راهبردهای درمانی دارد که در مراحل اولیه زنجیره التهابی عمل کنند.
References
1. Langan SM, Irvine AD, Weidinger S. Atopic dermatitis. Lancet. 2020;396(10247):345-360. doi:10.1016/s0140-6736(20)31286-1
2. Furue M, Furue M. OX40L-OX40 Signaling in Atopic Dermatitis. J Clin Med. 2021;10(12): 2578. doi:10.3390/jcm10122578
3. Weidinger S, Beck LA, Bieber T, Kabashima K, Irvine AD. Atopic dermatitis. Nat Rev Dis Primers. 2018;4(1):1. doi:10.1038/s41572-018-0001-z
4. Czarnowicki T, He H, Krueger JG, Guttman-Yassky E. Atopic dermatitis endotypes and implications for targeted therapeutics. J Allergy Clin Immunol. 2019;143(1):1-11. doi:10.1016/j.jaci.2018.10.032
5. Sadrolashrafi K, Guo L, Kikuchi R, et al. An OX-Tra’Ordinary Tale: The Role of OX40 and OX40L in Atopic Dermatitis. Cells. 2024;13(7): 587. doi:10.3390/cells13070587
6. Guttman-Yassky E, Simpson EL, Reich K, et al. Summary of Research: An Anti-OX40 Antibody to Treat Moderate-to-Severe Atopic Dermatitis: A Multicentre, Double-Blind, Placebo-Controlled Phase 2b Study. Adv Ther. 2024;41(3):928-931. doi:10.1007/s12325-023-02755-z
7. Croft M, Esfandiari E, Chong C, et al. OX40 in the Pathogenesis of Atopic Dermatitis-A New Therapeutic Target. Am J Clin Dermatol. 2024;25(3):447-461. doi:10.1007/s40257-023-00838-9
8. Croft M, So T, Duan W, Soroosh P. The significance of OX40 and OX40L to T-cell biology and immune disease. Immunol Rev. 2009;229(1):173-191. doi:10.1111/j.1600-065X.2009.00766.x
9. Ilves T, Harvima IT. OX40 ligand and OX40 are increased in atopic dermatitis lesions but do not correlate with clinical severity. J Eur Acad Dermatol Venereol. 2013;27(2):e197-205. doi:10.1111/j.1468-3083.2012.04587.x
10. Eiz-Vesper B, Schmetzer HM. Antigen-Presenting Cells: Potential of Proven und New Players in Immune Therapies. Transfus Med Hemother. 2020;47(6):429-431. doi:10.1159/000512729
11. Kim BE, Leung DYM. Significance of Skin Barrier Dysfunction in Atopic Dermatitis. Allergy Asthma Immunol Res. 2018;10(3):207-215. doi:10.4168/aair.2018.10.3.207
12. Tai Y, Wang Q, Korner H, Zhang L, Wei W. Molecular Mechanisms of T Cells Activation by Dendritic Cells in Autoimmune Diseases. Front Pharmacol. 2018;9:642.
13. Harryvan TJ, de Lange S, Hawinkels L, Verdegaal EME. The ABCs of Antigen Presentation by Stromal Non-Professional Antigen-Presenting Cells. Int J Mol Sci. 2021;23(1) 137. doi:10.3390/ijms23010137
14. Fu Y, Lin Q, Zhang Z, Zhang L. Therapeutic strategies for the costimulatory molecule OX40 in T-cell-mediated immunity. Acta Pharm Sin B. 2020;10(3):414-433. doi:10.1016/j.apsb.2019.08.010
15. Künzli M, Masopust D. CD4(+) T cell memory. Nat Immunol. 2023;24(6):903-914. doi:10.1038/s41590-023-01510-4
16. Noval Rivas M, Chatila TA. Regulatory T cells in allergic diseases. J Allergy Clin Immunol. 2016;138(3):639-652. doi:10.1016/j.jaci.2016.06.003
17. Sckisel GD, Bouchlaka MN, Monjazeb AM, et al. Out-of-Sequence Signal 3 Paralyzes Primary CD4(+) T-Cell-Dependent Immunity. Immunity. 2015;43(2):240-250. doi:10.1016/j.immuni.2015.06.023
18. Halim TYF, Rana BMJ, Walker JA, et al. Tissue-Restricted Adaptive Type 2 Immunity Is Orchestrated by Expression of the Costimulatory Molecule OX40L on Group 2 Innate Lymphoid Cells. Immunity. 2018;48(6):1195-1207.e6. doi:10.1016/j.immuni.2018.05.003
19. Hammad H, Lambrecht BN. Barrier Epithelial Cells and the Control of Type 2 Immunity. Immunity. 2015;43(1):29-40. doi:10.1016/j.immuni.2015.07.007
20. Vu MD, Xiao X, Gao W, et al. OX40 costimulation turns off Foxp3+ Tregs. Blood. 2007;110(7):2501-10. doi:10.1182/blood-2007-01-070748
21. Johnson BB, Franco AI, Beck LA, Prezzano JC. Treatment-resistant atopic dermatitis: challenges and solutions. Clin Cosmet Investig Dermatol. 2019;12:181-192. doi:10.2147/ccid.S163814
22. Lobefaro F, Gualdi G, Di Nuzzo S, Amerio P. Atopic Dermatitis: Clinical Aspects and Unmet Needs. Biomedicines. 2022;10(11):2927. doi:10.3390/biomedicines10112927
مطالعه بیشتر از طریق لینک زیر: